近日,IDEA 研究院与晶泰科技共同宣布,双方合作项目取得阶段性重要进展。IDEA 晶泰人工智能实验室开发了基于 AI 的高通量高精度抗体结构预测模型 idealFold,结合 IDEA 研究院强大的人工智能技术与算力资源,以及晶泰科技的下一代抗体发现平台 XupremAb™,将先进的 AI 算法与大分子药物研发专家经验有机结合,应用于抗体结构预测中。
经下游任务的湿实验验证,idealFold 的预测速度和预测精度均达到行业领先水平,高通量且高精度的抗体结构预测将对抗体理性设计、可开发性预测、超大抗体库构建等产生积极作用,大大提高了抗体药物的研发效率。这一成果标志着 IDEA 晶泰人工智能实验室在人工智能技术和应用研究方面取得重要突破,为未来抗体药物研发提供强有力的支持。
AlphaFold2 于 2021 年在蛋白质结构预测方面取得突破性进展,展示了 AI 在生命科学领域的应用潜力。虽然 AlphaFold2 可以利用不同蛋白间的多重序列比对(MSA),实现对未知蛋白质结构的预测[1],从进化的角度看,抗体并不存在 MSA 信息,较难通过 MSA 实现抗体结构的预测,因而 AlphaFold2 在抗体结构预测方面的准确率不够高,难以得到很好的应用落地。
AlphaFold2 的运行速度也极大地制约了其在工业界级别的药物发现中的落地。另外,AI 领域的干实验指标与药物研发领域的湿实验指标之间存在鸿沟,仅仅从 AI 角度进行算法改进常常是难以落地的。举例来说,抗体结构预测的 RMSD 等干实验指标的提升并不一定能让真实的药物研发获益。
为了解决抗体结构预测 AI 在大分子药物研发领域的落地难题,IDEA 晶泰人工智能实验室研发推出了第一代基于 AI 的抗体结构预测模型 idealFold。
首先,基于专家经验筛选的海量自然抗体数据库搭建了大型抗体预训练模型。其次,该模型利用大规模预训练模型从无标注蛋白质序列数据中学习到的表征为输入,搭配基于层次化聚类得到的蛋白质残基生化性质,建模蛋白质序列与空间结构的关系,避免了使用 MSA 作为输入,节省了多序列比对过程,极大地提升了模型推理的速度。
抗体结构 H3 区域的长度高度可变性、结构高度可变一直是抗体结构预测的难题,idealFold 通过引入多重位置编码信息,包括针对 CDR 区域的相对位置编码和绝对位置编码,增强了模型对抗体不同可变区的感知能力。idealFold 的单抗版本还集成了增强配对的特征表示,把抗体的轻重链位置信息也放入了配对特征表示中,提高了模型对轻链和重链的区分能力,从而提升模型性能。
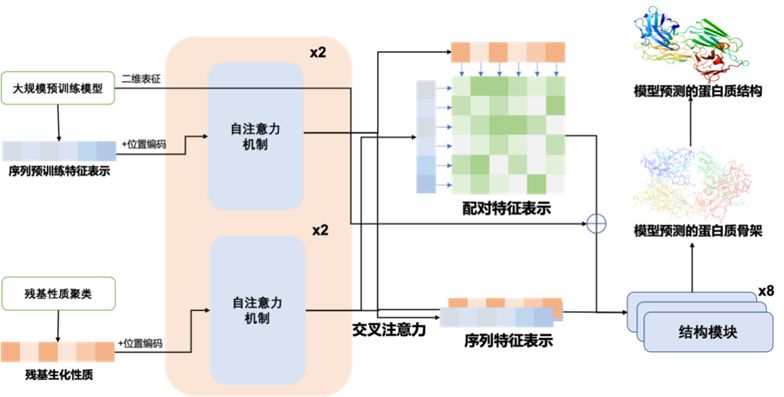 idealFold 模型架构图
idealFold 模型架构图
经过与同类模型分别在单抗和 VHH 抗体结构预测效果的比较,该模型的运行速度比当前行业广泛使用的 IgFold 快 93 倍,大大提升了 AI 算法预测抗体结构的效率。更进一步地,为了加速该模型的应用落地,IDEA 晶泰人工智能实验室将 idealFold 应用于晶泰科技下一代抗体发现平台 XupremAb™的 VHH 抗体的疏水性预测并进行了湿实验验证。结果表明,idealFold 的 Spearman 系数达 0.82,超过其他两个行业内的主流模型 OmegaFold(0.79)和 IgFold(0.70),在真实的大分子药物研发任务中崭露头角。
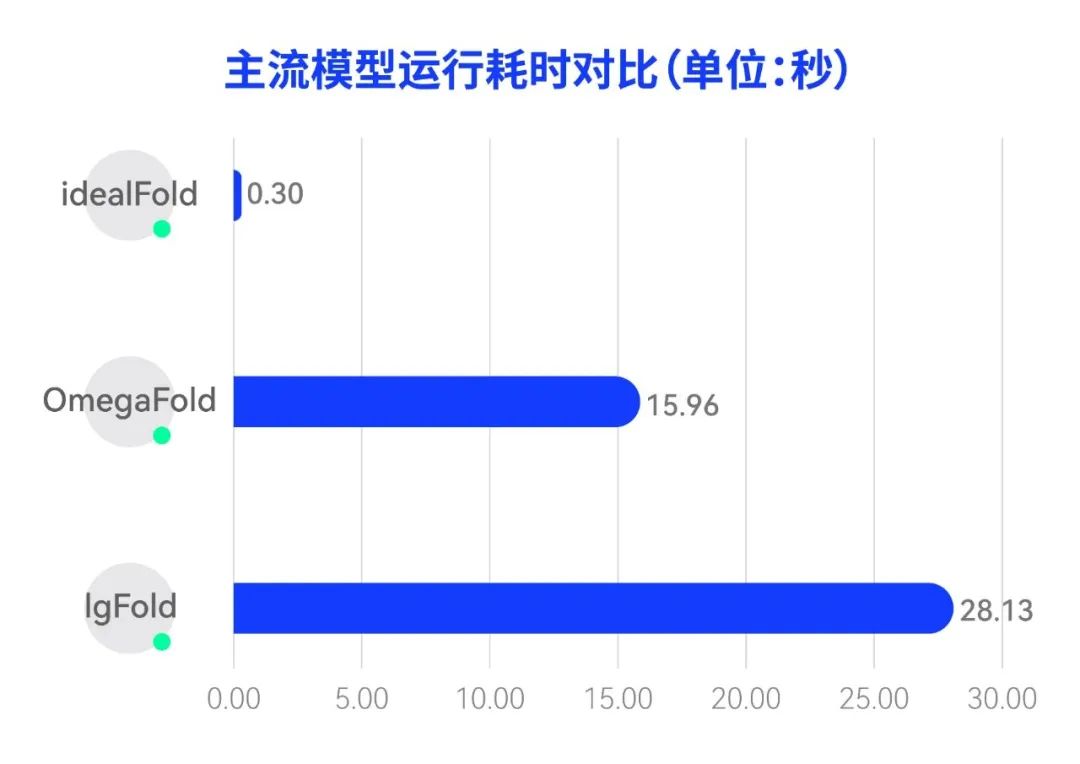 主流模型运行耗时对比图
主流模型运行耗时对比图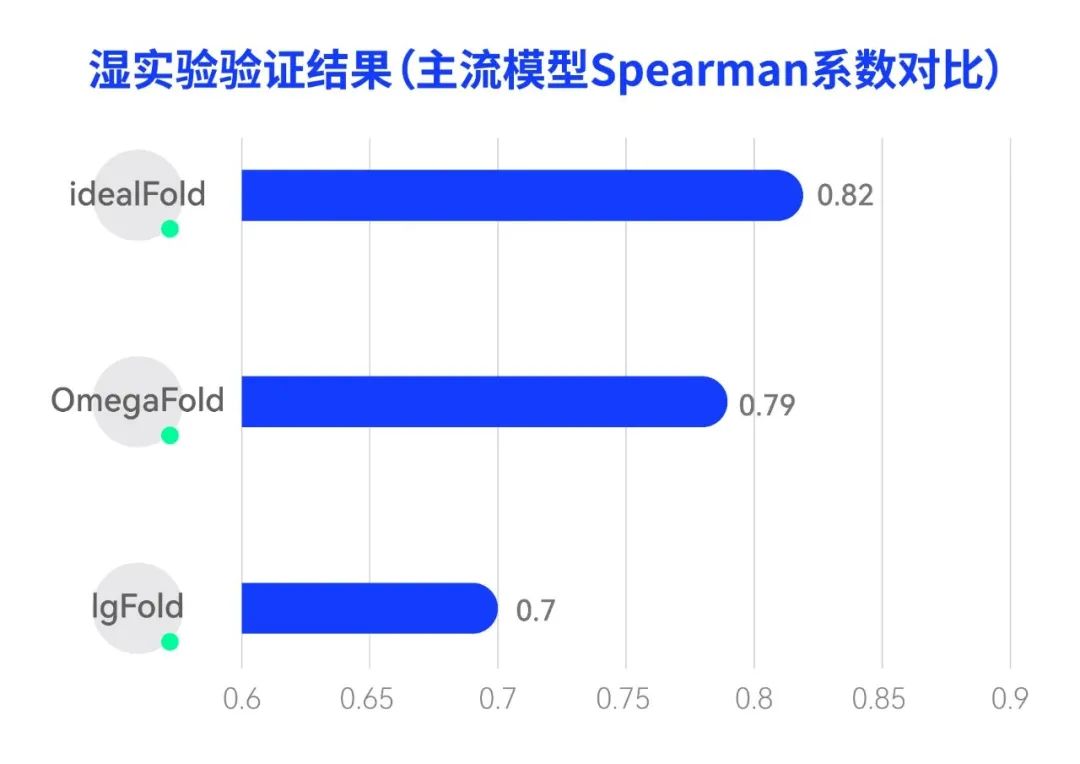 疏水性预测的湿实验验证结果对比图
疏水性预测的湿实验验证结果对比图
此次发布的 idealFold 模型,是 IDEA 晶泰人工智能实验室面向 AI 药物研发领域的一项重要突破。IDEA 研究院和晶泰科技于 2021 年合作成立 IDEA 晶泰人工智能实验室,是 CTO Labs 合作计划的重要组成部分。该计划旨在与全球领先的技术型独角兽企业合作,携手解决研产脱轨问题。IDEA 研究院致力于世界一流的科研,合作企业在各自领域为客户解决痛点,创造价值。目前合作计划进展顺利,包括数说故事实验室、视见睿来实验室、翼方健数实验室等均已有成熟的技术成果在合作企业的业务场景中落地和应用,帮助合作企业进一步提升了产品的市场竞争力。
IDEA 研究院联合实验室负责人幺宝刚表示:“我们正处于人工智能技术爆发的时代,AI 赋予了我们新的发展机遇。IDEA 研究院不仅专注于人工智能技术研究,而且更希望通过人工智能技术驱动各行各业的发展,让更多的人从数字经济发展中获益。其中,生物医药领域是近些年 AI 落地最直接的应用场景之一。我们很荣幸能与全球药物研发智能化、自动化的行业开拓者晶泰科技合作,期待利用我们在 AI 技术方面的优势,共同探索更广阔的大分子序列和结构空间,拓展产业边界,让 AI 赋能大分子药物发现。”
晶泰科技战略发展副总裁、抗体业务线负责人李一表示:“我们很荣幸与 IDEA 建立战略合作关系。AI 驱动大分子药物发现是晶泰科技近两年来积极部署的研究方向,致力于将人工智能技术和自动化前沿技术进一步拓展到大分子药物发现领域,提高大分子药物发现的新颖性和成功率。通过此次合作,我们希望进一步巩固晶泰科技在人工智能计算方面的领先优势,依靠晶泰科技在 AI 制药行业累积多年的算法落地经验,让 AI 在大分子药物研发领域的应用进一步落地,满足该领域仍未被满足的临床需求,让患者早日受益。”
参考文献:
[1] John Jumper et al, Highly accurate protein structure prediction with AlphaFold
近日,IDEA 研究院与晶泰科技共同宣布,双方合作项目取得阶段性重要进展。IDEA 晶泰人工智能实验室开发了基于 AI 的高通量高精度抗体结构预测模型 idealFold,结合 IDEA 研究院强大的人工智能技术与算力资源,以及晶泰科技的下一代抗体发现平台 XupremAb™,将先进的 AI 算法与大分子药物研发专家经验有机结合,应用于抗体结构预测中。
经下游任务的湿实验验证,idealFold 的预测速度和预测精度均达到行业领先水平,高通量且高精度的抗体结构预测将对抗体理性设计、可开发性预测、超大抗体库构建等产生积极作用,大大提高了抗体药物的研发效率。这一成果标志着 IDEA 晶泰人工智能实验室在人工智能技术和应用研究方面取得重要突破,为未来抗体药物研发提供强有力的支持。
AlphaFold2 于 2021 年在蛋白质结构预测方面取得突破性进展,展示了 AI 在生命科学领域的应用潜力。虽然 AlphaFold2 可以利用不同蛋白间的多重序列比对(MSA),实现对未知蛋白质结构的预测[1],从进化的角度看,抗体并不存在 MSA 信息,较难通过 MSA 实现抗体结构的预测,因而 AlphaFold2 在抗体结构预测方面的准确率不够高,难以得到很好的应用落地。
AlphaFold2 的运行速度也极大地制约了其在工业界级别的药物发现中的落地。另外,AI 领域的干实验指标与药物研发领域的湿实验指标之间存在鸿沟,仅仅从 AI 角度进行算法改进常常是难以落地的。举例来说,抗体结构预测的 RMSD 等干实验指标的提升并不一定能让真实的药物研发获益。
为了解决抗体结构预测 AI 在大分子药物研发领域的落地难题,IDEA 晶泰人工智能实验室研发推出了第一代基于 AI 的抗体结构预测模型 idealFold。
首先,基于专家经验筛选的海量自然抗体数据库搭建了大型抗体预训练模型。其次,该模型利用大规模预训练模型从无标注蛋白质序列数据中学习到的表征为输入,搭配基于层次化聚类得到的蛋白质残基生化性质,建模蛋白质序列与空间结构的关系,避免了使用 MSA 作为输入,节省了多序列比对过程,极大地提升了模型推理的速度。
抗体结构 H3 区域的长度高度可变性、结构高度可变一直是抗体结构预测的难题,idealFold 通过引入多重位置编码信息,包括针对 CDR 区域的相对位置编码和绝对位置编码,增强了模型对抗体不同可变区的感知能力。idealFold 的单抗版本还集成了增强配对的特征表示,把抗体的轻重链位置信息也放入了配对特征表示中,提高了模型对轻链和重链的区分能力,从而提升模型性能。
 idealFold 模型架构图
idealFold 模型架构图
经过与同类模型分别在单抗和 VHH 抗体结构预测效果的比较,该模型的运行速度比当前行业广泛使用的 IgFold 快 93 倍,大大提升了 AI 算法预测抗体结构的效率。更进一步地,为了加速该模型的应用落地,IDEA 晶泰人工智能实验室将 idealFold 应用于晶泰科技下一代抗体发现平台 XupremAb™的 VHH 抗体的疏水性预测并进行了湿实验验证。结果表明,idealFold 的 Spearman 系数达 0.82,超过其他两个行业内的主流模型 OmegaFold(0.79)和 IgFold(0.70),在真实的大分子药物研发任务中崭露头角。
 主流模型运行耗时对比图
主流模型运行耗时对比图 疏水性预测的湿实验验证结果对比图
疏水性预测的湿实验验证结果对比图
此次发布的 idealFold 模型,是 IDEA 晶泰人工智能实验室面向 AI 药物研发领域的一项重要突破。IDEA 研究院和晶泰科技于 2021 年合作成立 IDEA 晶泰人工智能实验室,是 CTO Labs 合作计划的重要组成部分。该计划旨在与全球领先的技术型独角兽企业合作,携手解决研产脱轨问题。IDEA 研究院致力于世界一流的科研,合作企业在各自领域为客户解决痛点,创造价值。目前合作计划进展顺利,包括数说故事实验室、视见睿来实验室、翼方健数实验室等均已有成熟的技术成果在合作企业的业务场景中落地和应用,帮助合作企业进一步提升了产品的市场竞争力。
IDEA 研究院联合实验室负责人幺宝刚表示:“我们正处于人工智能技术爆发的时代,AI 赋予了我们新的发展机遇。IDEA 研究院不仅专注于人工智能技术研究,而且更希望通过人工智能技术驱动各行各业的发展,让更多的人从数字经济发展中获益。其中,生物医药领域是近些年 AI 落地最直接的应用场景之一。我们很荣幸能与全球药物研发智能化、自动化的行业开拓者晶泰科技合作,期待利用我们在 AI 技术方面的优势,共同探索更广阔的大分子序列和结构空间,拓展产业边界,让 AI 赋能大分子药物发现。”
晶泰科技战略发展副总裁、抗体业务线负责人李一表示:“我们很荣幸与 IDEA 建立战略合作关系。AI 驱动大分子药物发现是晶泰科技近两年来积极部署的研究方向,致力于将人工智能技术和自动化前沿技术进一步拓展到大分子药物发现领域,提高大分子药物发现的新颖性和成功率。通过此次合作,我们希望进一步巩固晶泰科技在人工智能计算方面的领先优势,依靠晶泰科技在 AI 制药行业累积多年的算法落地经验,让 AI 在大分子药物研发领域的应用进一步落地,满足该领域仍未被满足的临床需求,让患者早日受益。”
参考文献:
[1] John Jumper et al, Highly accurate protein structure prediction with AlphaFold
